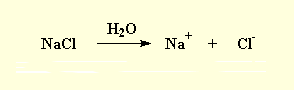پلی الکترولیت چیست؟ معرفی انواع پلی الکترولیت ها
پلی الکترولیت ها لخته کننده ها و منعقد کننده هایی هستند که به دو صورت جامد و مایع با هدف لخته کردن مورد استفاده قرار می گیرند. این ماده شیمیایی در سه گروه کاتیونی ، آنیونی و غیر یونی دسته بندی می شود که در ادامه بیشتر توضیح داده خواهد شد. در واقع خاصیت لخته کنندگی پلی الکترولیت سبب شده است که این ماده کاربرد بسیاری در صنایع تصفیه آب داشته باشد.
| خرید پلی الکترولیت
شرکت شیمیایی بوعلی سینا یکی از بزرگترین وارد کنندگان پلی الکترولیت و منعقد کننده ها در کشور می باشد. شما میتوانید برای خرید منعقد کننده با کارشناسان ما در ارتباط باشید. شماره های تماس : 02188502389 – 02188748404 |
پلی الکترولیت چیست ؟
همانطور که گفته شد پلی الکترولیت ها در واقع پلیمرهایی هستند که توسط مکانیسم تولید یون به مولکول پلیمری در سراسر زنجیره تبدیل می شوند و در واقع پلی الکترولیت ها ، الکترولیت هایی هستند که هم خاصیت پلیمری دارند هم خاصیت الکترولیت.
انواع پلی الکترلیت ها
منعقدکننده ها و کمک منعقد کننده به به انواع مختلف طبیعی و مصنوعی و یونی تقسیم می شوند که در ادامه به صورت کامل توضیح داده شده است.
1- پلی الکترولیت های طبیعی
متداول ترین این مواد عبارتند از : پکتین (اسید پلی گالاکترونیک)،آلژینات(اسیدآلژنیک)،کربوکسی متیل سلولز و پلی پپتیدها.
2- پلی الکترولیت های مصنوعی
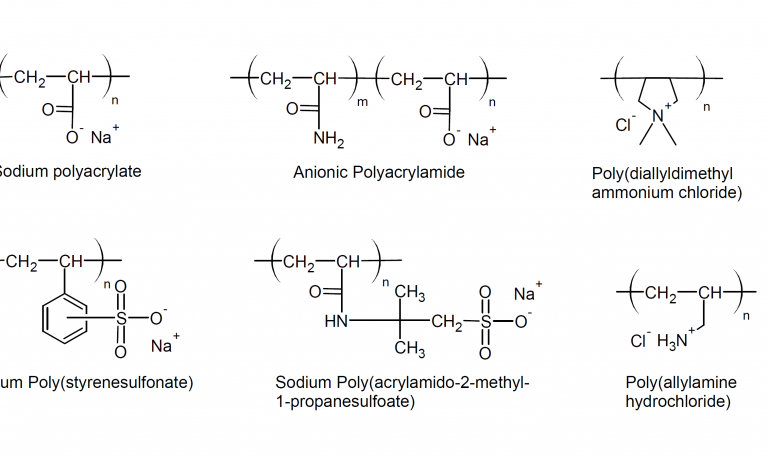
متداول ترین این مواد عبارتند از : پلی اکریلیک اسید ، پلی استایرن سولفانات ، پلی الیل امین ، کربوکسی متیل سلولز و نمک های این ها.
توجه داشته باشید که هر دو پلی اتیلن طبیعی و مصنوعی در مقیاس بزرگ تولید می شوند . بعضی از این پلی الکترولیت ها در زیر نشان داده شده است.
3- پلی یون ها
برخی دیگر از این ترکیبات شامل گروه های باردار در زنجیره اصلی هستند.این دسته از مواد بعنوان پلی یون ها شناخته میشوند. رایج ترین گروه باردار در زنجیره اصلی آمونیوم نوع ۴ است. این پلی آمین های یونی به طور معمول از طریق یک واکنش منشوتکین از آمین های طبقه ای و دی آلیدهای آلکیل تولید می شوند.
سنتز پلی یون ها
تعداد زیادی دی هالید و آمین های وابسته به صورت تجاری در دسترس هستند که باعث سنتز تعداد زیادی از پلی یونی ها شده است و از مواد اولیه نسبتاً ارزان و یک مسیر سنتز نسبی ساده می شود. هر دو فاصله یونی روی زنجیره اصلی پلیمر ، یعنی چگالی بار و وزن مولکولی به راحتی قابل تنظیم است. علاوه بر این ، بسیاری از گروه های عملکردی دیگر را می توان به راحتی درج کرد ، که امکان اتصال متقابل خصوصیات فیزیکی و مکانیکی را فراهم می آورد.
بیشتر بخوانید: بهترین آنتی اسکالانت چیست؟
گروه های پلی الکترولیت ها
پلی الکترولیت ها بعنوان منعقد کننده و کمک منعقدکننده در تصفیه آب و فاضلاب شناخته میشوند، این مواد پلیمری توسط پل زنی شیمیایی میتوانند مواد معلق در آب را جدا نمایند و به منعقد کننده ها کمک میکنند. کاتیون یا آنیون متصل به پیکره شیمیایی پلی آکریل آمید تعیین کننده نوع بار فعال پلیمر میباشد که این مواد براساس اینکه نوع یونیزه شده ی آن ها در آب چه نوع باری را حمل میکند به انواع گوناگونی تقسیم میشوند.
بارهای مثبت(cationic) منفی(anionic) و بدون بار(non-ionic) تقسیم میشوند:
1- پلی الکترولیت آنیونی(Anionic Polyelectrolytes)
سه گروه متداول پلی الکترولیت آنیونی عبارتند از : کربوکسیلات (-COO-) ، فسفنات ها (-PO3H-,PO32-) ، و سولفانات ها (-SO3-)
کوپلیمرهای آکریل آمید با خواص ارتقاء یافته باری توسط گروههای سدیم آکریلات هستند، بار منفی داشته و پس از انحلال در آب، محلول با خواص بار منفی ایجاد میکنند.
2- پلی الکترولیت کاتیونی(Cationic Polyelectrolyte)
آمونیوم نوع اول ، دوم و ۴م (-NH3+,=NH2+,&=-N+ )
کوپلیمرهای آکریل آمید به همراه مونومرهای کاتیونی بوده که باعث ارتقاء بار مثبت در این دسته از پلیمرها میشوند و پس از انحلال در آب، محلول با خاصیت باری مثبت ایجاد میکنند. نوع گروه یونی و مونومر های سازنده و واحد تکرارشونده پلی الکترولیت ، خواصی چون حلالیت در آب و دیگر مایعات پیوند قطبی و پیوند هیدروژن (الکلها و غیره)، هدایت الکتریکی و ویسکوزیته محلول را تعیین میکند.
3- پلی الکرتولیت خنثی/بدون بار (Non-Ionic Polyelectrolytes)
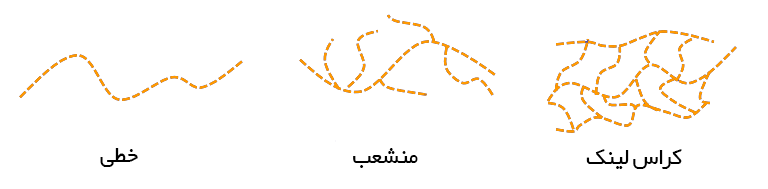
این گروه بر پایه پلی آکریل آمیدخالص میباشند و پس از حل شدن در آب از خود خاصیت بدون بار نشان میدهند.خواص پلیمرهای خنثی به شدت PH و مقدار نمک بستگی دارد.با وارد کردن مقدار کمی از یک ماده اتصال مناسب ، می توان پلی الکترولیت ها را به صورت شیمیایی متصل کرد. این مواد میتوانند با پیوند عرضی شیمیایی(کراس لینک) بوسیله مقدار کمی از عامل های متصل کننده محلول ترکیب شوند.
این ترکیبات دارای ساختار ۳بعدی هستند که بجای انحلال در آب ، متورم میشوند.آنها می توانند مقادیر زیادی مایع نسبت به جرم خود از طریق پیوند هیدروژن با مولکول های آب حفظ کنند که به آن ها هیدروژل یا پلیمرهای سوپر جاذب(SAP) میگویند. توانایی آن ها برای جذب آب عاملی برای غلظت یونی محلول های آبی است.در آب دیونیزه شده و مقطر SAP ها ( سوپر جاذب ها) آب را تا ۵۰۰ برابر وزن خود و از ۳۰تا۶۰ برابر حجم خود جذب کنند یعنی یک هیدروژل میتواند بیش از ۹۹% مایع تشکیل دهد.قدرت جذب و تورم کل SAP با توجه به نوع و میزان خط مقطع موجود در ساختار کنترل میشود.
بیشتر بخوانید : تولید پلی آلومینیوم کلراید | معرفی روش و فرآیند تولید
خواص پلی الکترولیت ها
پلی الکترولیت ها دارای خواص مختلفی هستند که در ادامه برخی از آن ها توضیح داده شده است :
1- تبدیل لخته های کوچک به صورت لختههای درشت و سنگین
این مواد دارای خواص پلیمر و الکترولیتی بوده ، که این خاصیت میتواند اندازه لخته را درشتتر نماید.
2-افزایش سرعت عمل ته نشینی و کاهش حجم لجن تشکیل شده
بارهای موجود در ساختار این ترکیب ایجاد یک میدان قوی الکتروستاتیک میکند که اثر قابل توجهی بر روی ساختار مولکول میکند. یعنی به طور قابل توجهی شکل های ماکرومولکولی را تغییر می دهد .
3-افزایش درجه تفکیک و کاهش مقدار مصرف ماده منعقد کننده با گسترش بهینه محدود PH
اندازه زنجیر ها افزایش می یابد. هنگامی که درجه تفکیک تغییر میکند خصوصیات فیزیکی و شیمیایی دچار تغییرات قابل توجهی میشود به عنوان مثال، ویسکوزیته محلول بسته به غلظت پلی الکترولیت در محلول ، درجه تفکیک آن و غلظت یون آزاد ( نمک ) ( یونهای با وزن کم مولکولی موجود در محلول ) می تواند با ضریب صد و بیشتر افزایش یابد.
تولید پلی الکترولیت
همانطور که گفته شد این ماده شیمیایی در دو نوع جامد و مایع وجود دارد برابراین می توان آن را به دو صورت مایع یا جامد تولید کرد. پلی الکترولیت توسط گروه آمید (NH۲) از نظر شیمیایی پلیمر را اصلاح می کند تا پلیمر کاتیونی با بار مثبت یا پلیمر آنیونی با بار منفی تولید گردد. بهعنوان بخشی از فرایند تولید، میتوان ویژگیهای یونی پلیمر را دستکاری کرد تا درجات مختلفی شامل نوع آنیونی و نوع کاتیونی و نوع غیریونی حاصل شود که این یک عامل کلیدی در انتخاب نوع پلیمر است.
ساختار مولکولی پلی الکترولیت
ساختار مولکولی این مواد طبق عکس زیر می باشد.
گریدبندی پلی الکترولیت
در جدول های زیر گریدهای مختلف پلی الکترولیت بر اساس نوع کاتیونی و آنیونی معرفی شده است.
پلی الکترولیت آنیونی
| A500 | grade |
| Anionic | A500 |
| million20 | Molcular weight |
| fast &complete | Water soluble |
| white granule | Appearance |
| water & waste water | Application |
پلی الکترولیت کاتیونی
| A500 | grade |
| cationic | A500 |
| million4-10 | Molcular weight |
| white dry powder | Appearance |
| water & waste water | Application |
کاربردهای پلی الکترولیت
پلی الکترولیت ها در صنایع مختلف کاربردهای گوناگونی داند که در ادامه بعضی از آن ها توضیح داده شده است:
۱- کمک منعقد کننده در فرآیند زلال سازی آب خام برای تولید آب آشامیدنی و صنعتی
بعنوان منعقد کننده درتولید آب آشامیدنی و صنعتی در فرایند زلال سازی آب خام در صنایع مختلف که فرایند کریستالیزاسیون دارند مانند تولید نمک ها کریستال خوراکی و صنعتی در فرایند تولید کاغذ و شیت های یونولیت
۲- منعقد سازی جامدات معلق و کلوئیدها در فرآیندهای شکر و تغلیظ مایعات
منعقد کننده ذرات جامد معلق و کلوییدها در تغلیظ مایعات
۳- جداسازی جامدات و ترکیبات آلی در آب برگشتی سیستمهای تبرید و حرارتی
جهت جداسازی جامدات ، روغن و گریس و اکسیدهای نامحلول در تصفیه آب برگشتی از بخش نورد در صنعت فولاد برای حذف رنگ ، مواد جامد معلق و کلویید ها
۴- منعقدکننده در سیستمهای تصفیه پسابهای صنعتی و بهداشتی
در صنایع تولید محصولات پتروشیمی به عنوان منعقد کننده در سیستم های تصفیه پساب های صنعتی و بهداشتی جهت جداسازی هم زمان ذرات سبک چربی و روغن و جداسازی ذرات سنگین در صنایع پالایشگاهی و پتروشیمی (تکنولوژی DAF) از آنجا که این ترکیب و کمک منعقد کننده ها ، مواد جاذب رطوبت شدید هستند ، از برخی گونه در بخش کشاورزی برای جذب آب و بالا بردن ضریب جذب آب خاک استفاده می شود.
در نهایت استفاده از این ترکیب سبب کاهش قابل توجه مصرف مواد منعقد کننده مانند پلی آلومینیوم کلراید شده و لذا از لحاظ اقتصادی نقش مهمی در کاهش هزینه مواد مصرفی تصفیه خانه دارد.
بیشتر بخوانید : هیدرازین چیست (N2H4)؟ | فرمول مولکولی و شیمیایی هیدرازین
تفکیک در آب
الکترولیت ها نیز دوست دارند از هم تفکیک شوند فقط کافیست آن ها را در آب ریخته تا سریعا به یون های خود تجزیه شوند مثل نمک طعام NaCl که یک نوع الکترولیت ضعیف است و اگر آن را در اب بریزید به یون های سدیم مثبت و کلر منفی تجزیه میشود.
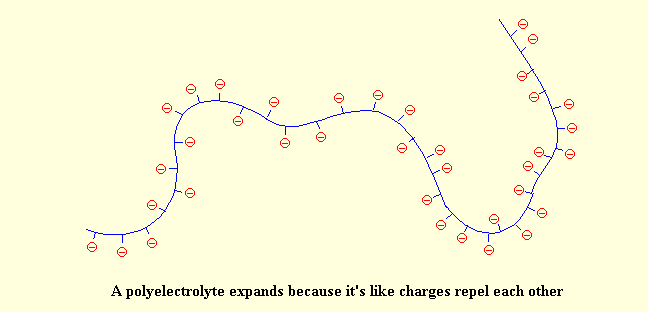
پلی الکترولیت ها در ابتدا به صورت زنجیره های مارپیچ هستند
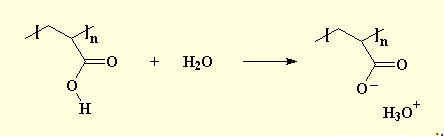
اما با اضافه کردن پلی اکریلیک اسید در آب ، هیدروژن های اسیدی جدا شده و با مولکول های آب بون های H3O+ را تشکیل میدهند:
پس از تشکیل H3O+ پلیمر با بار منفی در محلول باقی میماند و بارهای منفی تمایل به دفع یکدیگر دارند و نمیتوانند شکل مارپیچی خود را حفظ کنند در نتیجه به صورت شکل زیر در می آیند:
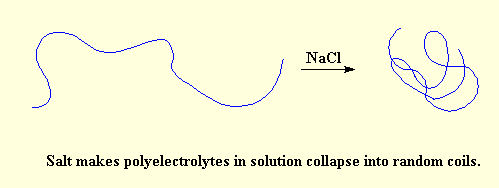
هنگامی که این زنجیره به صورت خطی گسترده میشود فضای بیشتری را اشغال میکند و در برابر جریان مولکول های حلال اطراف خود مقاوم تر عمل میکند و باعث ویسکوز شدن و غلیظ تر شدن محلول میشود. برای رفع این مشکل در محلول پلی الکترولیت یونی با بار منفی مانند پلی (اکریلیک اسید) مقداری نمک افزوده و نمک به یون های Na+ و Cl- تجزیه میشود و یون های سدیم مثبت بین بارهای منفی پلیمر وارد میشوند و اثر دافعه یون ها را خنثی میکنند و زنجیره پلیمری مجددا به شکل مارپیچ تصادفی در می اید.
مکانیسم منعقد سازی پلی الکترولیت
گروههای فعال پلیمر در محیط آبی، پیوند قوی با کلوئیدهای معلق یا ذرات بسیار ریز ایجاد مینمایند. در پلیمرهای نانیونیک ، فعل و انفعال بین پلیمر و ذرات معلق وابسته به باندهای هیدروژن آنها داشته و فعالیت پلیمرهای باردار (کاتیونیک و آنیونیک) وابسته به برخوردهای الکترواستاتیک و تبادل بار بین ذرات معلق و پلیمر و ناپایداری خصوصیت سطح ذرات میباشد.